4月19日����,中國科學技術大學微尺度物質科學國家研究中心曾杰教授和耿志剛教授研究團隊,在《自然·可持續性》(Nature Sustainability)發表了題為“Synthesis of hydroxylamine from air and water via a plasma-electrochemical cascade pathway”的文章����。該研究提出了等離子體-電化學級聯催化新模式�����,僅以空氣和水作為反應物��,以電能為驅動力�,在常溫常壓條件下實現了羥胺的綠色可持續合成�����。

羥胺作為一種重要的化工中間體����,被廣泛應用于醫藥����、農藥、紡織、電子等精細化工領域。羥胺的衍生物作為纖維穩定劑和芯片清洗劑在紡織和電子領域被普遍使用����。羥胺的傳統生產方法主要包含拉西法��、一氧化氮還原法和硝酸還原法。然而,拉西法以高腐蝕性和重污染性的二氧化硫作為還原劑,在生產羥胺的過程中會產生大量硫酸氨副產品,在導致大量的氮流失的同時,會造成環境污染�����;一氧化氮還原法和硝酸還原法需在鉑�����、鈀等貴金屬材料催化下�,以氫氣作為還原劑和氫源���,成本昂貴����,還會在生產過程中產生大量碳排放��。面對羥胺傳統生產工藝存在的諸多弊病���,亟需開創一種綠色����、低碳���、可持續的羥胺合成新工藝��。
以綠色電能為驅動力�����、以水為質子源的電合成過程有望克服傳統羥胺生產工藝的弊端。然而�,受限于氮氣分子的熱力學穩定性���,氮氣的直接電催化還原/氧化過程難以實現氮氣分子的高效活化��。為突破氮氣直接電化學活化的低活性限制,本工作采用等離子體固氮策略,以空氣作為反應物,將其通過等離子體高壓放電活化為氮氧化物,再利用水作為氮氧化物吸收劑��,制得硝酸溶液�。接著,通過催化劑設計,將硝酸溶液經過陰極選擇性還原制得羥胺���,其反應過程與優勢如圖1所示。本工作通過開發等離子體固氮制硝酸耦合硝酸電催化還原制羥胺級聯反應新工藝,實現了僅以空氣和水為原料、綠色可持續合成羥胺的研究目標�。
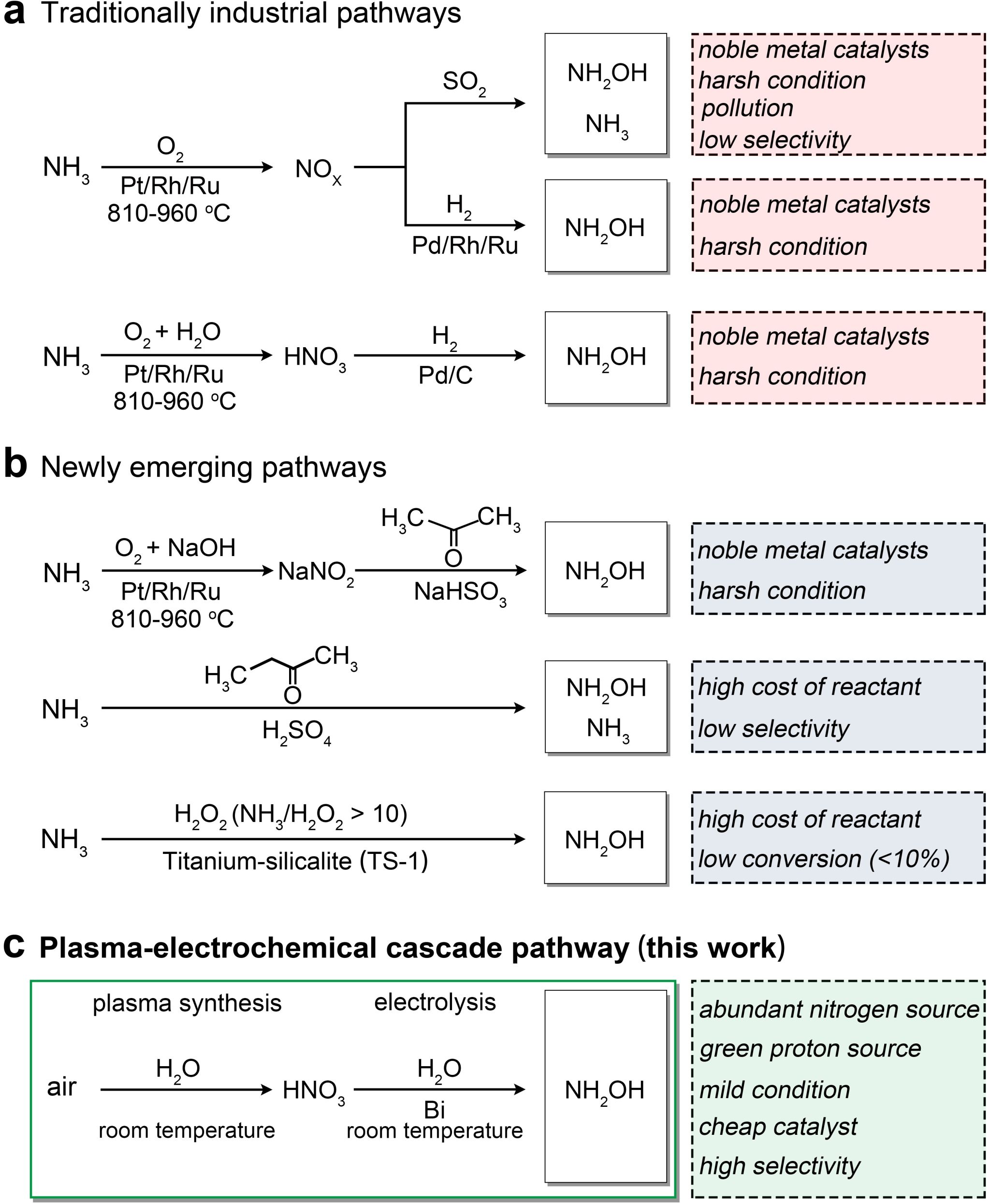
圖1 等離子體放電耦合電催化還原制羥胺新工藝反應過程示意圖及其優勢
氮氣分子的高效活化與轉化是實現氮物種資源化利用的前提���。研究人員受“雷雨發莊稼”自然現象啟發���,設計出等離子體平行電弧放電裝置�,從而實現氮氣的高效活性���。首先���,研究人員將空氣通入等離子體平行電弧放電裝置��,并利用含甲基橙的水溶液作為尾氣吸收劑����,在30秒尾氣吸收過程中��,溶液由橙黃色變為紫紅色�,說明溶液由中性轉變為酸性����。通過優化空氣流速,經過5分鐘吸收過程即可獲得最高濃度達20.3毫摩爾每升的硝酸溶液。經過30分鐘電弧放電和尾氣吸收過程��,可獲得高達120.1毫摩爾每升的硝酸溶液����。以每30分鐘為一輪反應,該等離子體放電裝置在20輪循環反應過程中保持優異的穩定性����,如圖2所示���。上述所得硝酸溶液經稀釋和添加電解質后可直接用于電催化合成羥胺的過程����。
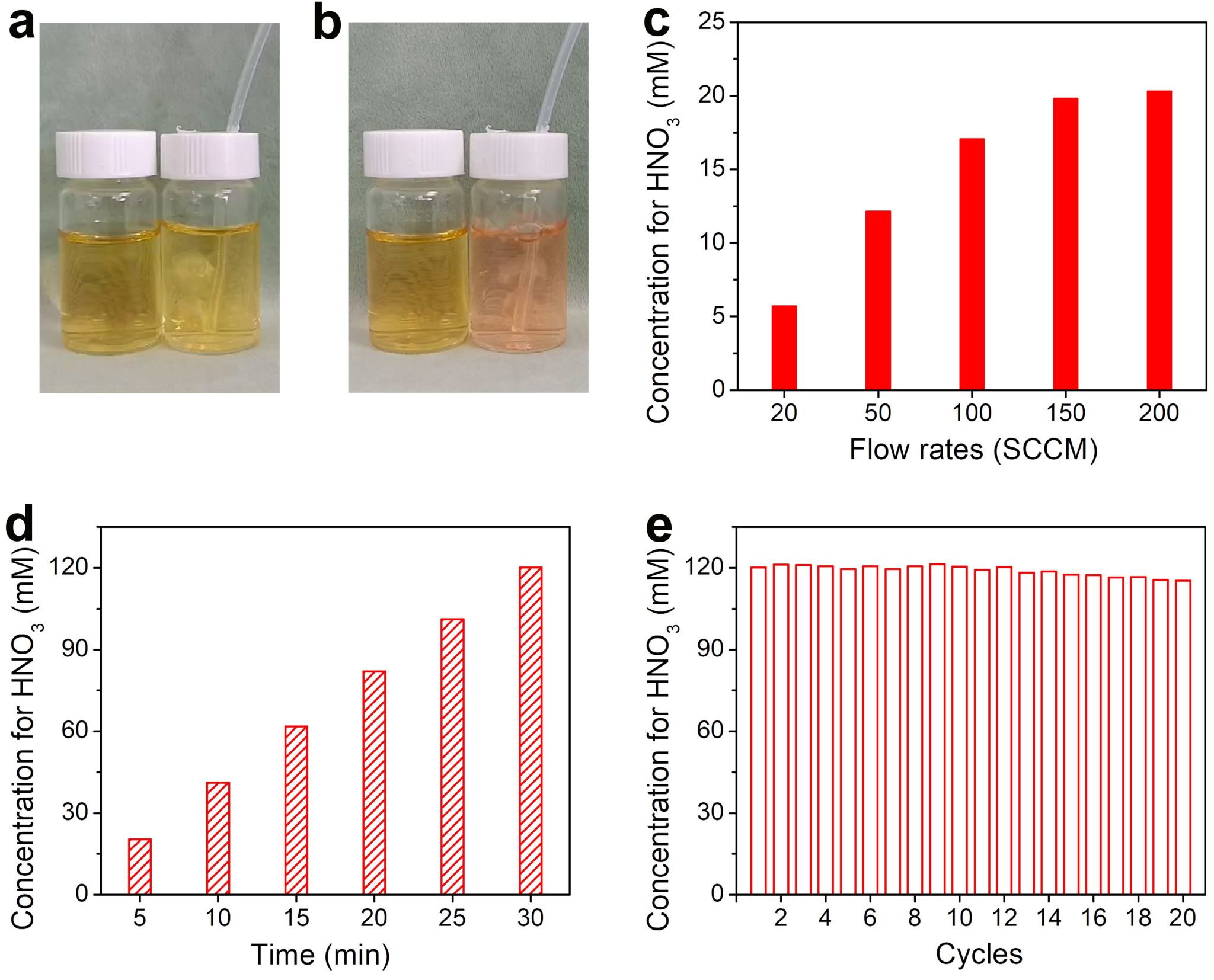
圖2等離子體放電制備高純硝酸溶液
研究人員以碳紙作為基底����,通過磁控濺射法制得金屬鉍薄膜催化劑�����,并將其應用于電催化硝酸還原制羥胺反應���?����;阢G基材料的高析氫過電位,鉍薄膜催化劑對電催化硝酸還原制羥胺展現出高達80.1%的電流效率和96.6%的羥胺產物選擇性��。當施加相對標準氫電極-1.2伏的陰極電位時�,羥胺產率高達713.1微摩爾每平方厘米每小時。接著���,研究人員探究了鉍薄膜催化劑長時間電解100毫摩爾每升硝酸溶液時,羥胺在電解液中的累積過程���。經過5小時連續電解,羥胺的最高濃度達到77.7毫摩爾每升�����。將鉍薄膜催化劑應用于循環穩定性測試�����,每輪連續電解5小時�����,經過12輪電解過程��,羥胺的產物選擇性依然高達95.7%���。研究人員收集12輪循環穩定性后的電解液���,經過除雜�、濃縮和冷卻結晶,獲得1.887克高純硫酸羥胺產品,如圖3所示�。
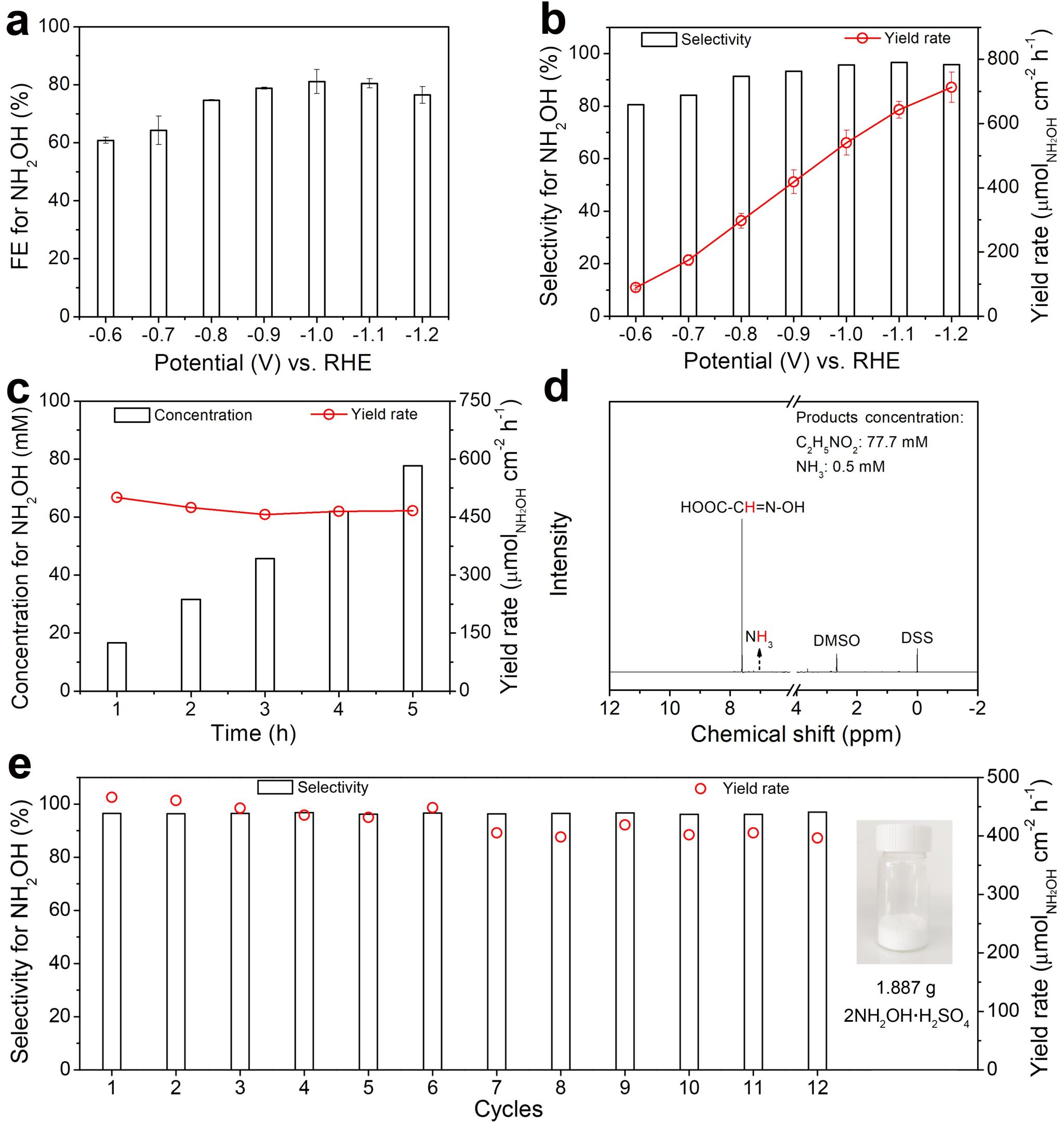
圖3 金屬鉍薄膜電催化硝酸還原制羥胺的性能
研究人員進一步探究了鉍基催化劑電催化硝酸還原制羥胺的催化反應機理�。對反應路徑分析結果表明���,制備羥胺的另一關鍵在于吸附態羥胺分子在催化劑表面的吸附行為:當羥胺分子在催化劑表面呈現弱吸附時����,吸附態羥胺分子可直接脫附得到游離態羥胺;反之�,催化劑對羥胺分子的強吸附將導致羥胺分子進一步質子耦合電子轉移形成終態還原產物氨���。研究人員借助理論模擬��,證實在金屬鉍表面吸附態羥胺分子的脫附易于吸附態羥胺分子的解離,并且����,析氫反應勢壘遠高于硝酸還原制羥胺速控步反應勢壘�。結合理論模擬�����,研究人員進一步對多種催化材料進行了性能篩選�,發現相較于其他催化材料體系�����,鉍基催化劑對吸附態羥胺分子易脫附難解離的特性,是其高活性高選擇性電合成羥胺的主要原因�,其機理探究如圖4所示�����。
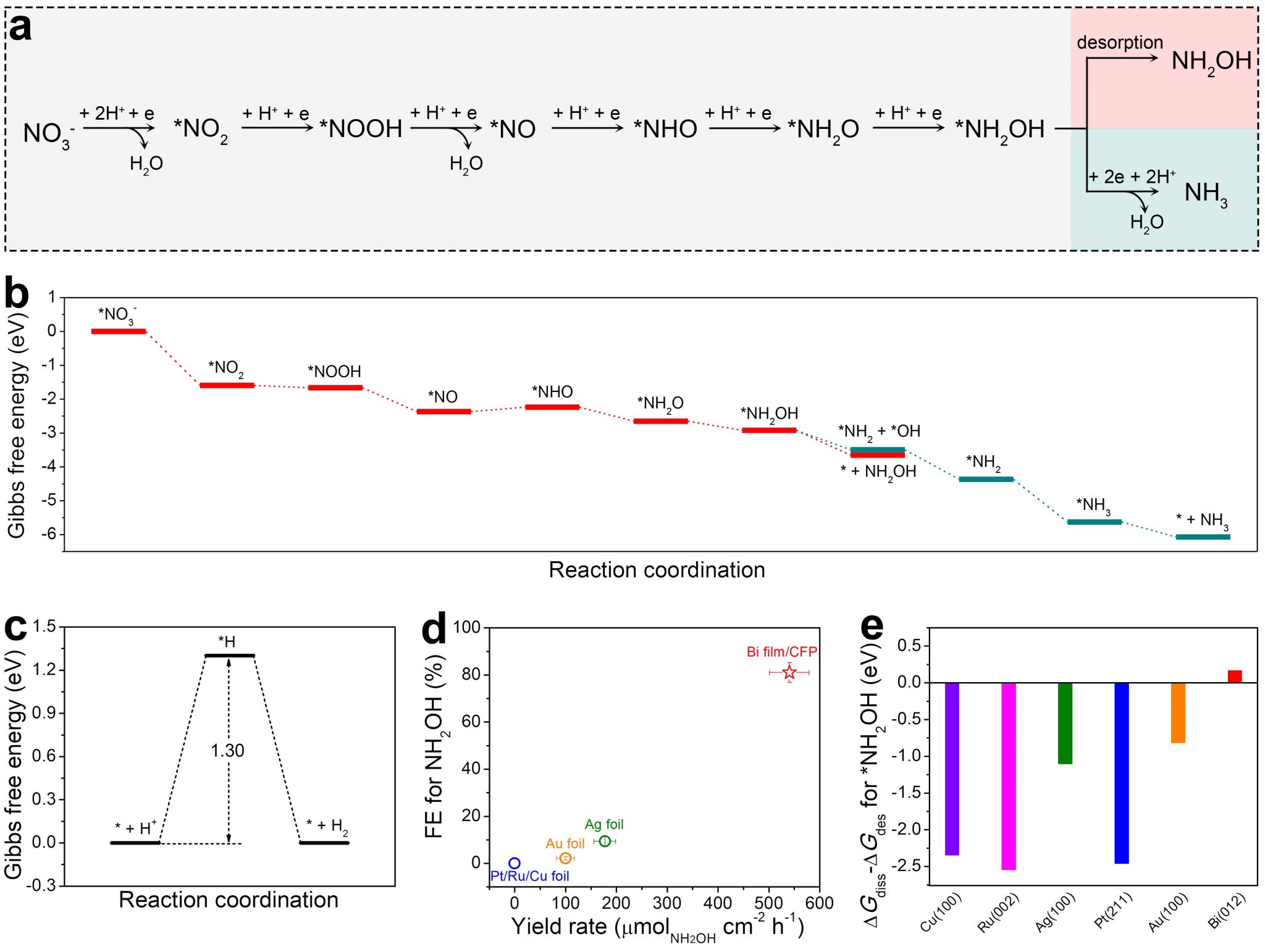
圖4 鉍基催化劑選擇性電催化硝酸還原制羥胺的機理探究
此項工作得到中國科學院先導專項、國家自然科學基金��、科技部重點研發等項目的支持����。特任副研孔祥棟和博士生倪潔為共同第一作者,曾杰教授和耿志剛教授為通訊作者。
論文鏈接:https://www.nature.com/articles/s41893-024-01330-w
(合肥微尺度物質科學國家研究中心����、科研部)

