大腦衰老過程中會產生結構上的退行性改變,以及功能衰退。大腦結構的改變主要表現為大腦皮層體積的縮小,該變化主要影響運動、心理活動等執行功能。被稱為大腦細胞的“能量工廠”線粒體,其主要以ATP的形式為神經元提供能量,維持神經元的神經遞質合成、軸突運輸以及有氧代謝等過程的能量需求。然而,線粒體在大腦衰老進程中,結構發生明顯的退行性改變,功能發生明顯的下降。然而,衰老過程中線粒體結構和功能改變的調控機制仍不清楚。衰老是阿爾茨海默病最重要的風險因素,認知功能障礙和線粒體結構功能異常也是阿爾茨海默病的重要病理特征,但是衰老如何導致阿爾茨海默病的發生發展并不清楚。
近日,中國科學技術大學劉強團隊揭示了在衰老和阿爾茨海默病的大腦中會產生大量的谷氨酸tRNA片段,并在線粒體內發生異常累積,導致線粒體蛋白的翻譯發生損傷以及內嵴結構發生破壞,最終損傷谷氨酸的合成過程,加速大腦衰老和阿爾茨海默病的病理進程。相關研究成果以題為“Aging-induced tRNAGlu-derived fragment impairs glutamate biosynthesis by targeting mitochondrial translation-dependent cristae organization”發表在在《Cell Metabolism》雜志上。
在這篇論文中,研究人員首先發現谷氨酸tRNA片段在大腦衰老進程中,其表達水平顯著上升,并且這種增加具有物種保守性。除了衰老的大腦,在阿爾茨海默癥病人的大腦中也同樣檢測到谷氨酸tRNA片段的增加。進一步的研究表明,谷氨酸tRNA片段的產生是依賴于angiogenin(ANG):ANG在衰老過程中從細胞核異常定位到細胞質,并對谷氨酸tRNA進行切割。
研究人員利用分子雜交以及免疫熒光等技術發現谷氨酸tRNA片段主要在谷氨酸能神經元中的線粒體內發生異常積累。通過RNA-pull down和蛋白質譜的方法鑒定了谷氨酸tRNA片段的結合蛋白-線粒體亮氨酸氨酰化合成酶(LaRs2)。研究人員利用生化實驗和透射電鏡技術發現谷氨酸tRNA片段和線粒體亮氨酸tRNA競爭性結合LaRs2,破壞線粒體亮氨酸tRNA的氨酰化以及線粒體蛋白的翻譯過程,進一步損傷線粒體內嵴結構以及谷氨酰胺酶依賴的谷氨酸的合成過程,進而加速大腦衰老的進程。
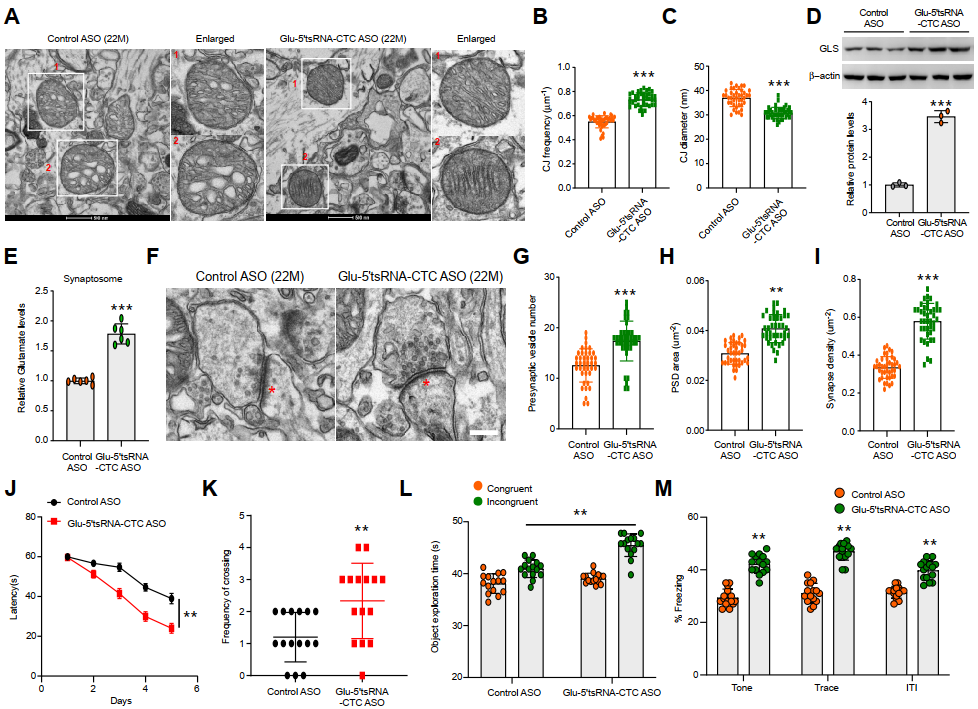
圖1. tRNA片段的功能調控
設計靶向該tRNA片段的反義寡核苷酸,并注射到衰老小鼠的大腦內,可以通過恢復谷氨酸能神經元中線粒體的蛋白翻譯,內嵴結構,以及腦谷氨酸水平,顯著減輕衰老小鼠學習記憶障礙。這些研究結果進一步支持谷氨酸tRNA片段是加速大腦衰老的重要風險因子,這也為減緩腦衰老相關的學習記憶功能障礙提供了新的治療靶點。
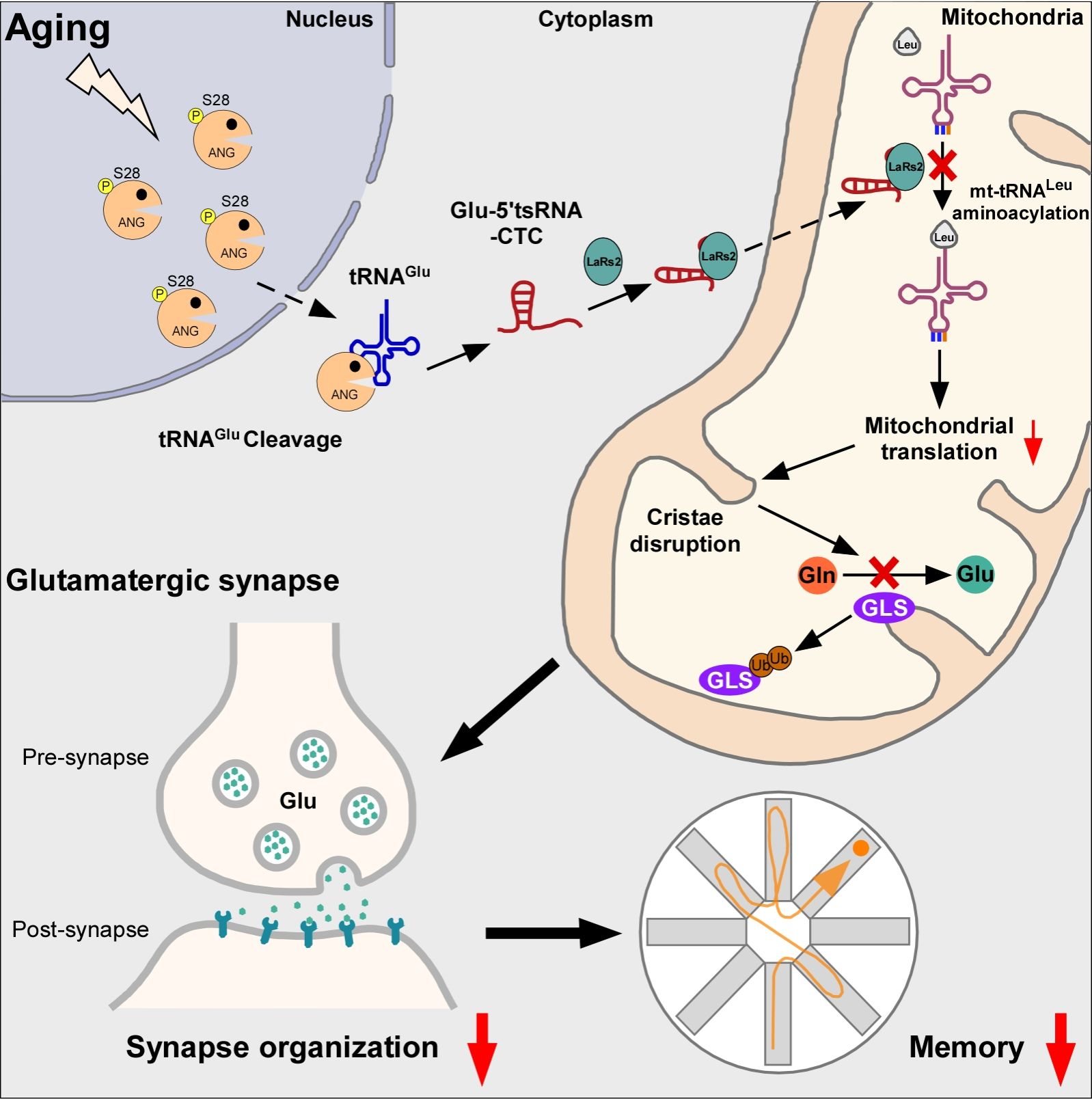
圖2. tRNA片段在腦衰老和阿爾茨海默病中調控機制示意圖
綜上,這項研究揭示了在腦衰老和阿爾茨海默病中異常積累的谷氨酸tRNA片段通過損傷線粒體的蛋白翻譯過程和內嵴結構,抑制谷氨酸的合成,進而加速大腦衰老和阿爾茨海默病的病理進程。該項研究對理解大腦衰老與阿爾茨海默病的發病機制具有重要意義,揭示了tRNA片段在大腦衰老中的全新作用,并且提出了延緩認知衰退的治療新思路。
中國科學技術大學特任副研究員李定豐為論文的第一作者,劉強教授為論文的通訊作者。本研究也得到了中國科學技術大學申勇教授,薛天教授,汪銘教授的大力支持,以及實驗中心任繼樹和施榮華兩位老師的幫助。
文章鏈接:https://doi.org/10.1016/j.cmet.2024.02.011
(生命科學與醫學部、科研部)

