
<ul id="aocae"></ul> <ul id="aocae"></ul> 
日期:2023-04-24點擊:
中國科學技術大學生命科學與醫學部孫寶林教授課題組揭示了金黃色葡萄球菌一氧化氮合成酶NOS及其內源產生的NO通過介導靶蛋白的S-亞硝基化修飾以調控萬古霉素耐藥性發生的具體分子機制。研究成果以“Transcription tuned by S-nitrosylation underlies a mechanism forStaphylococcus aureusto circumvent vancomycin killing”為題于4月21日在線發表在《Nature Communications》雜志上。
金黃色葡萄球菌(Staphylococcus aureus)是人類主要致病細菌,由甲氧西林耐藥性金黃色葡萄球菌(methicillin-resistantS. aureus,MRSA)引發的感染正嚴重威脅公共健康安全。萬古霉素被認為是臨床上治療嚴重MRSA感染的最后一道防線,但是,其中度耐藥性金黃色葡萄球菌(vancomycin-intermediateS. aureus,VISA)的頻繁出現,為MRSA的感染治療帶來了巨大挑戰。因此,深入解析金黃色葡萄球菌萬古霉素耐藥機制具有重要的臨床意義。一氧化氮(nitric oxide,NO)可作為信號分子,首先在真核生物中被發現可由一氧化氮合成酶(nitric oxide synthase,NOS)內源產生,參與調節各種生理及免疫功能。NO被報道能對蛋白質半胱氨酸殘基的巰基進行S-亞硝基化修飾,進而影響蛋白質的活性和功能。金黃色葡萄球菌中也被證實存在可以催化產生NO的NOS,該酶被報道參與調控金黃色葡萄球菌的萬古霉素耐藥性,但相關分子機制尚不明確。
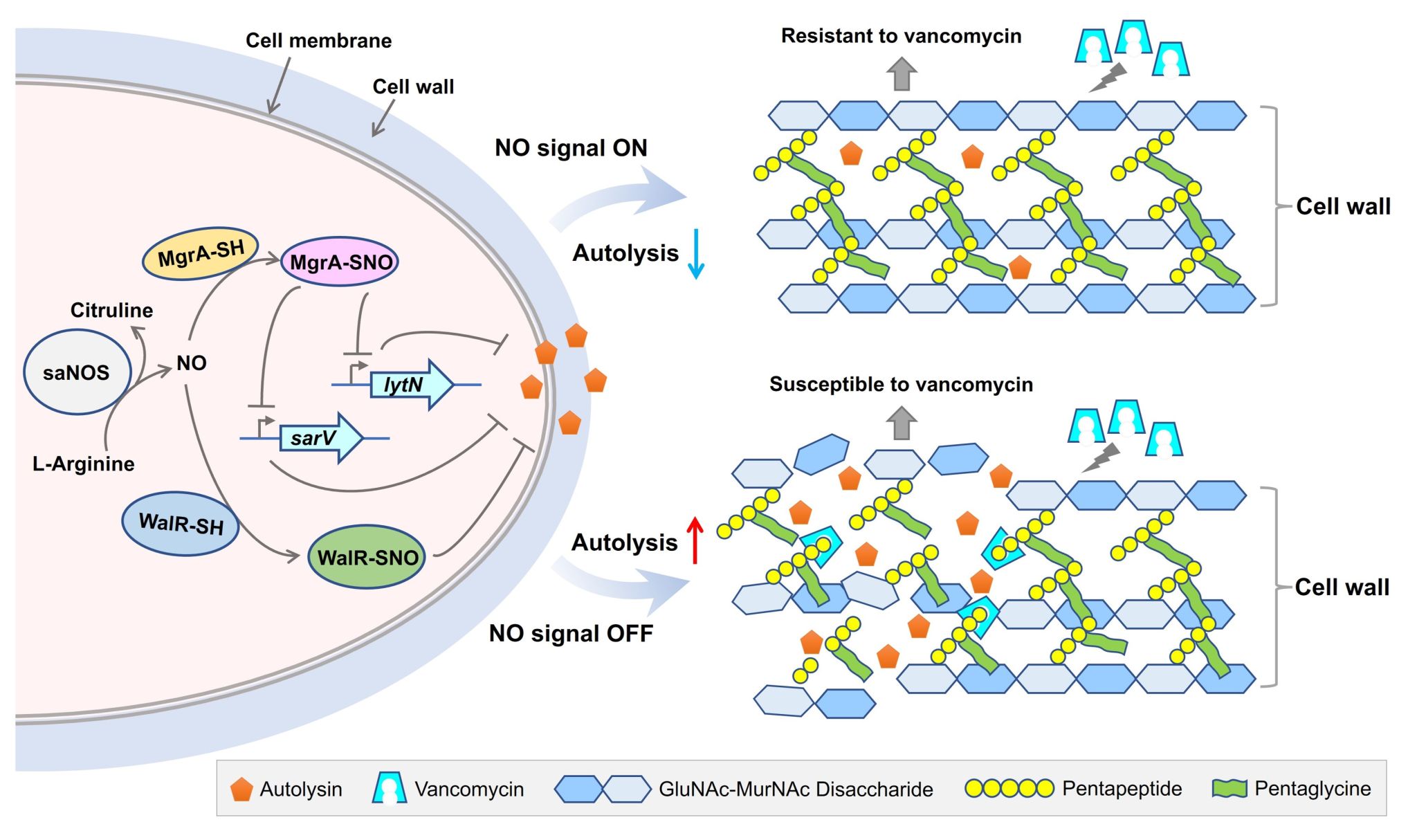
圖1. NOS通過S-亞硝基化修飾介導萬古霉素耐藥性的分子機制。當存在內源NO時,MgrA和WalR發生S-亞硝基化修飾(SNO),促進對自溶相關靶基因的負調控功能,導致細胞的自溶活性下降,介導細胞壁厚度增加,進而促進金黃色葡萄球菌的萬古霉素耐藥性。
研究人員在臨床VISA菌株XN108中,通過構建NOS突變菌株以及外源添加NOS抑制劑,證實了金黃色葡萄球菌NOS在萬古霉素等細胞壁靶向抗生素抗性發生過程中的重要作用。接下來,利用蛋白質修飾組學的方法鑒定了金黃色葡萄球菌中可被內源NO亞硝基化修飾的靶標蛋白及相應位點。一個與抗生素抗性具有重要關聯的轉錄因子MgrA上第12位的半胱氨酸發生了S-亞硝基化修飾,通過將半胱氨酸替換為不能被修飾的絲氨酸構建了mgrAC12S點突變菌株,發現NOS突變菌株類似,mgrAC12S突變菌株對萬古霉素的抗性顯著下降、細胞壁厚度顯著下降以及細胞自溶活性增加。通過實時熒光定量PCR、凝膠阻滯遷移實驗、染色質免疫共沉淀實驗等方法,揭示了金黃色葡萄球菌NOS及其內源產生的NO在促進萬古霉素抗性中的作用機制(圖1):NOS來源的NO通過介導MgrA發生S-亞硝基化修飾,促進MgrA對自溶相關靶基因的負調控功能,導致細胞的自溶活性下降,介導細胞壁厚度增加,進而促進金黃色葡萄球菌的萬古霉素耐藥性。這種由NO介導的調控機制在另一個被鑒定到可發生S-亞硝基化修飾的轉錄因子WalR中得到了進一步的驗證,表明金黃色葡萄球菌NOS內源產生的NO通過S-亞硝基化修飾介導的轉錄調控機制在細菌中可能具有普遍性。本研究有望為臨床治療VISA及其他細菌病原體的感染提供新的思路與策略。
本論文第一作者為孫寶林教授課題組的博士研究生舒雪琴,通訊作者為中國科學技術大學孫寶林教授和北京兒童醫院的于丹副研究員。該工作得到了科技部國家重點研發計劃、國家自然科學基金、中國科學技術大學中央高校基本科研業務費專項基金等項目的資助。
原文鏈接:https://www.nature.com/articles/s41467-023-37949-0
(生命科學與醫學部、科研部)